4-ALKENLER (Olefinler)
Alkenler yapılarında C=C karbon-karbon çift bağları içeren bileşiklerdir ve bunlara olefinler de denir, yaygın olarak kullanılan isim alkenlerdir. Alkenler tabiatta birçok yerde karşımıza çıkar ve bunların birçoğu da biyolojik aktiviteye sahiptir. Örnek olarak etilen bitkilerdeki olgunlaşmayı sağlayan bir bitki hormonudur ve a-pinenler deki tadı veren maddedir.
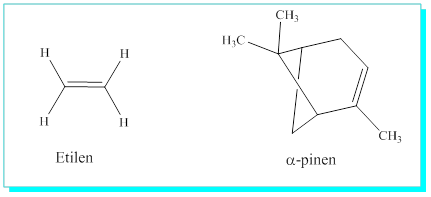
Havuca sarımsı rengi veren madde, b-kroten aynı zamanda Vitamin A’nın -temel yapısıdır, vitaminler olmadan hayatın olması söz konusu değildir ki b-krotenin bazı tür kanserleri önleyici özellikleri olduğu bilinmektedir.
4.1-Alkenlerin hazırlanışı ve bazı kullanıldığı yerler.
Alkenler birçok diğer organik kimyasalın çıkış (başlangıç) maddesi olduğundan etilen ( eten) ve propilen (Propen) başka maddeleri hazırlamada kullanılmak üzere çok miktarda üretilmektedir. Sanayide hazırlanışları gaz ( gaz yağı) nın, ki daha önce C4-C6 karbon içeren alkanlar olduğu açıklanmıştı, ısıl parçalanma denilen 850-900 °C ye kader ısıtılması ile elde edilirler.
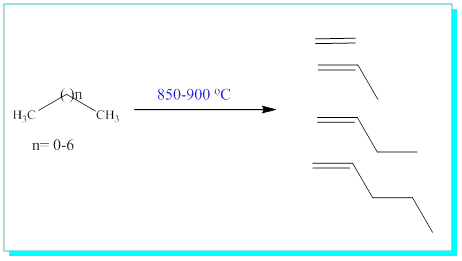
4.2-Eliminasyon (Ayrılma) ile Alken sentezi.
Laboratuvar şartlarında ise genelde alkol ve alkil halojenürlerin eliminasyonu yöntemleri ile sentezlenirler. Eliminasyon büyük bir molekülden iki atom ya da gurubun ayrılarak yeni moleküller vermesine denir. Alkilhalajenürlerden eliminasyon, bir hidrojen ve bir halojenin ayrılıp asit ve alken vermesi, alkollerde ise bir hidrojen ve bir hidroksil gurubunun ayrılarak su ve alken vermesi şeklindedir.
\ Örnek olarak,

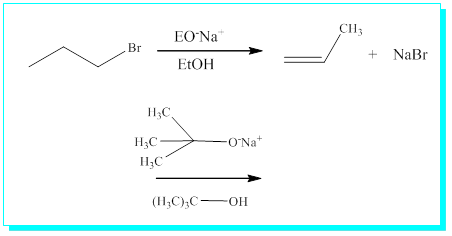
Eğer halojenin bağlı bulunduğu karbon ortada ise, karşımıza iki veya daha fazla ürün çıkma ihtimalide vardır. Bu durumu kısaca açıklarsak,
2-Bromo-2-metilbutanın eliminasyonu bize, 2-metil-2-buten ve 2-metil-1-buten olmak üzere iki çeşit ürün verir.
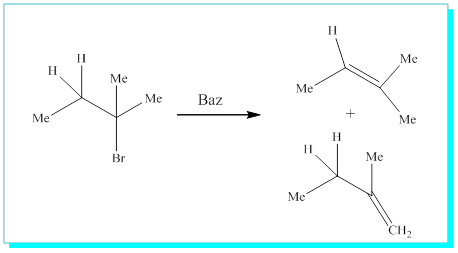
Burada bilinmesi gereken bazın halojene yakın olan bir protonu almasıdır ki, mümkün iki farklı tür hidrojen vardır. Bunlardan biri etil gurubunun, diğeri ise metil gurubunun hidrojenidir.
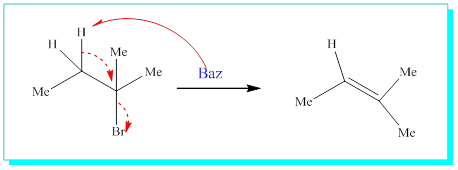
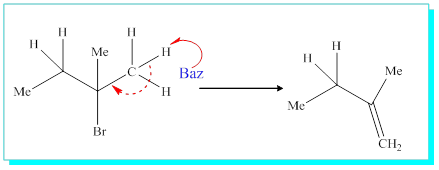
4.3-Alkollerin Eliminasyonu İle Elken Eldesi
Birçok alkolün güçlü asidik ortamda ısıtılması bir mol su ayrılması ile alkenleri verir.

Asit olarak çoğunlukla sülfürik asit ya da fosforik asit kullanılır.
Örnek olarak etil alkolün sülfürik asitle 180 °C ye ısıtılması eten verir.

Bu yöntemle prapanol ve etanolden sadece birer ürün elde ederken, alkilhalojenürlere benzer olarak büyük moleküllü alkollerin eliminasyonunda da çeşitli ürünlerin karışımını elde ederiz.
Bütanol için,
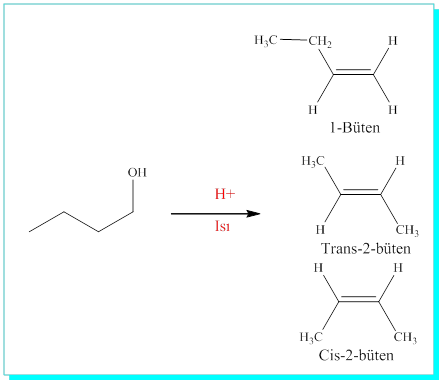
2-metilsiklohekzanol de 1-Metilsiklohexen ve 3-metilsiklohekzen olmak üzere iki ürün verir.
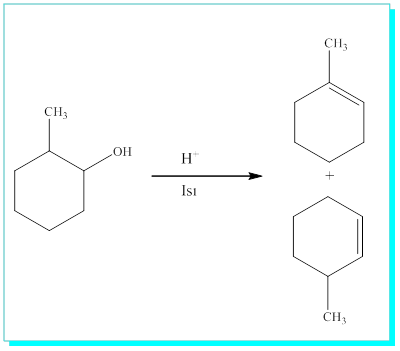
4.4-Karbokatyon Oluşumu Ve Kararlılığı
Uygulama:
1-C3H4 için mümkün olan tüm açık yapıları yazınız.
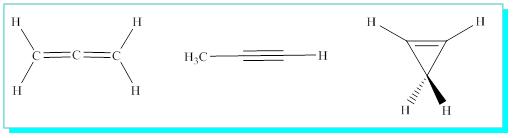
2-C4H6 için mümkün olan tüm açık yapıları yazınız.
Öğrenciye bırakılmıştır- 9-tanedir.
3- Aşağıdaki bileşiklerin hangilerinde Konjuge bağ vardır?
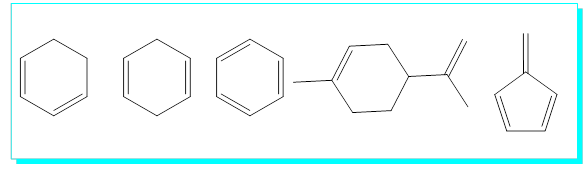
S/ Aşağıdaki bileşikleri adlandırınız.
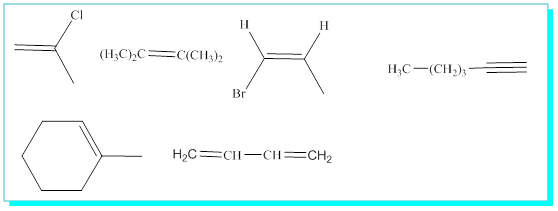
S/ 3-Metil-2-penten'in açık formülünü yazınız.
a) Penten beş karbonludur. C-C-C-C-C
b) 2-penten : çift bağ ikinci karbondadır. C-C=C-C-C
c) 3-metil : 3 numaralı karbona metil bağlıdır.

S/ 2,3-dimetil-2-penten'in açık formülünü yazınız.
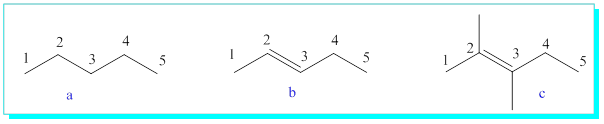
S/ Aşağıdaki ismi verilen moleküllerin açık formüllerini yazmayı da siz deneyiniz.
a) 3-hexin
b) 1,2-diklorosiklobuten
c) 2-bromo1-3-butadien
d) cis-1,2-dikloroeten
e) trans-1-chloropropen
S / 1-Buten ve siklopenten’e brom katılması reaksiyon denklemlerini yazınız.
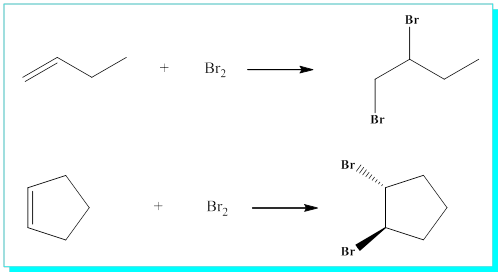
Alkenlere brom katilması reaksiyonları alkenlerin tanınma reaksiyonlarından da biridir. Bromun karbontetraklorür çözeltisi sarı renkli olmasına rağmen, alkene katılmada bu renk kaybolur. Kesin belirleyici olmamakla birlikte alkenlerin tanınmasında kullanılan bir yöntemdir.
4.5-Alkenlere Su (H2O) Katılması
Suyun asidik ortamda alkenlere katılması alkolleri verir. Genel olarak bu reaksiyon aşağıdaki gibi yazılabilir.

Örnek olarak, siklohezene asidik ortamda su katılması siklohekzanol verir.
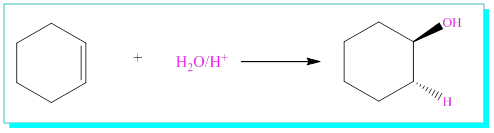
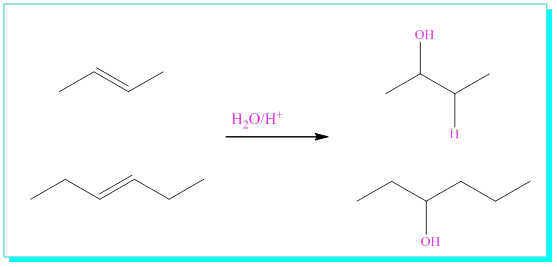
S/ 2-Buten ve 3-hexen’e asidik ortamda su katılması reaksiyonlarını yazınız.
4.6-Alkenlere Asit Katılması
Alkenler asit katılma reaksiyonu da verir bunlardan, hidrojen içerenlerde asidik hidrojen çift bağın bir tarafına bağlanırken diğer tarafına asidin artakalan anyonik kısmı bağlanır.

Asit olarak, HCl, HI, HBr, H-OSO3H, H-O-CO-R genelde kullanılanlardır.
Örneğin, Eten’e HBR katılması,

Siklopentenle sülfürik asidin reaksiyon denklemini ise,
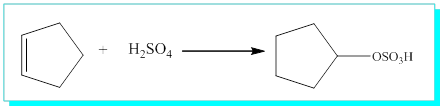
S / Aşağıdaki reaksiyon denklemlerini tamamlayınız.
a) 2-Buten + HI---------------->
b) Siklohezen+ HBr------------>
4.7-Markofnikof Kuralı
Alkenlere katılmalarda, eğer alken ve katılan gruptan her ikisi de simetrik değilse (asimetrik) hidrojen ve geri kalan kısmının alkenin hangi tarafına bağlandığı önem arz eder. Burada oluşma ihtimali olan iki tane molekül ortaya çıkar.
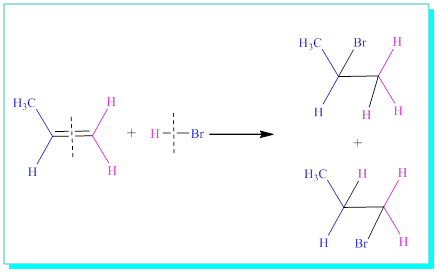
Görüldüğü gibi, bir defasında hidrojen CH3 ve bir hidrojenin bağlandığı karbon atomuna bağlanırken, diğerinde ise iki hidrojen atomunun bağlı bulunduğu karbon atomuna bağlanmıştır.
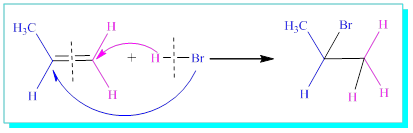
Markofnikof Ürünü (ana-asıl-ürün)
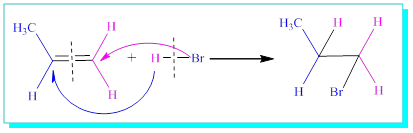
Anti-Markofnikof Ürünü (oluşmaz-ya da çok çok az oluşur)
Bu reaksiyonun laboratuvar şartlarında yapılması sonucunda sadece (II) numaralı reaksiyon ürününün oluştuğunu (I) numaralı reaksiyonunsa oluşmadığı gözlenir.
Burada dikkat edilirse hidrojen, hidrojenin çok olduğu yere (iki tane H) bağlanmıştır. Brom ise hidrojenin az olduğu yere (bir tane H) bağlanmıştır.
Bu durum genel bir kural olarak, Markofnikof kuralı diye bilinir.
Markofnikof kuralı: Asimetrik Alkenlere halojen asitlerinin katılması esnasında elektropozitif kısım (Hidrojen atomu) hidrojen atomunun çok olduğu yere bağlanır.
Bağlanmanın belli bir yere olduğu bu tür reaksiyonlara regiospesifik- yer seçimli- reaksiyonlar denir. Yani, Markofnikof kuralı regiospesifik bir reaksiyondur, hidrojen ve diğer gurubun nereye bağlanacağı önceden belirlenebilir.
S / Propen’e su katılması reaksiyonunu yazıp, oluşan ürünü isimlendiriniz.
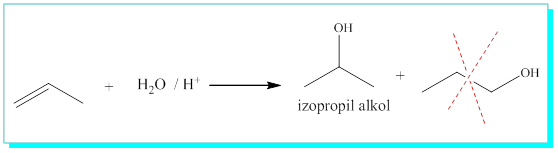
2-hidroksipropanol-, izo- ikinci karbona bağlı bulunan metil substituentleri için özel bir adlandırmadır. Bu bir regiospesifik reaksiyondur ve burada 1-propanol ya da diğer adı ile n-propanol oluşmaz.
Propen’e hidroklorik asit katılması da benzer şekilde sadece 2-kloropropen verir.
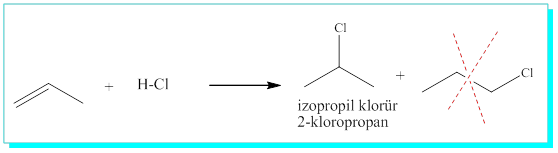
S / Aşağıdaki ürünlerden hangisinin oluşacağını tahmin ediniz?
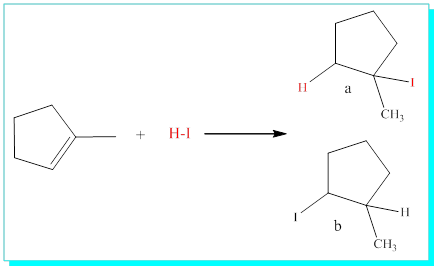
Hatırlatma, eğer bir asimetrik reaktif bir asimetrik alkene katılıyorsa, elektro pozitif kısım hidrojenin fazla olduğu yere bağlanır.
Burada asimetrik reaktiflerde polarlık olduğu anlamına gelir ki, Elektrofil ve Nüklefil diye isimlendirilen iki kısım ortaya çıkar.
Bunlardan;
Elektrofil, Latince elektron seven anlamına gelir, genelde pozitif (+) yüklü yada elektron alma eğiliminde bulunan boş orbitale sahiptirler. E+ olarak genel gösterime sahiptir ve reaksiyona gireceği molekülün tabi olarak elektronca zengin (-) kısmını tercih eder.
Nükleofil, Latince çekirdek seven anlamına gelip genelde negatif (-) yüklüdür, elektron çifti bulunduran ya da elektronca zengin orbitaller içeren yapı, Nü- şeklinde gösterime sahip ve reaksiyona gireceği molekülün elektronca fakir pozitif kısmını tercih eder.
Reaksiyonlar, elektrofil yada nükleofilin başlatması ile oluşur bunlar, eğer elektrofilin başlattığı reaksiyonsa, elektrofilik reaksiyon , nükleofilin başlattığı reaksiyon ise nükleofilik reaksiyon adını alır.
Alkenlere katılma reaksiyonları genelde elektrofilik katılmadır ve pozitif kısım ilk önce katılır, ikinci basamakta ise asidin geri kalan kısmı oluşan karbokatyona bağlanır.
Asit katılmasını örnek olarak alalım;
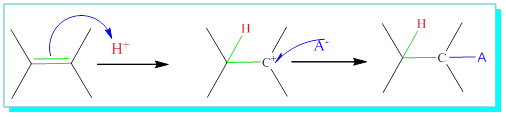
Markofnikof katılmasının mekanizması da bu şekilde açıklanabilir.
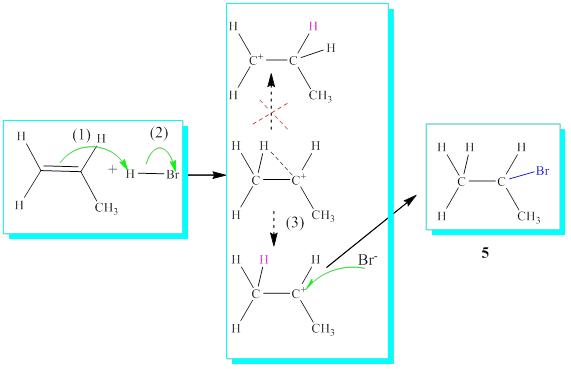
Mekanizmada 1-numaralı ok işareti, ilk önce alkenin çift bağının protona atak yaptığını ve 2-numaralı ok işareti ise bromun her iki elektronu alarak eksi (-) yüklü ayrıldığını göstermektedir. Oluşan karbokatyon köprülü şekilde veya açık şekilde olabilir. 3-numaralı ok işareti ile bromun hidrojenin bağlandığı yönün ters tarafından bağlanması ve köprünün açılması ile trans katılma tamamlanmış ve ürün -5- oluşmuştur.
Reaksiyon denkleminden de görüleceği üzere hidrojen hidrojenin çok olduğu yere bağlanmıştır.
Markofnikof katılmasında oluşan karbokatyon kararlılığı da büyük önem arz eder. Bilindiği gibi karbokatyon kararlılığı tersiyer > sekonder > primer şeklinde değişir.
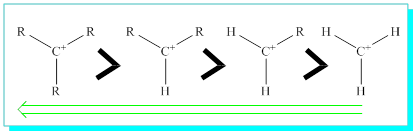
Bu durumu 2-metilpropene hidroklorik asit katılması ile inceleyelim.
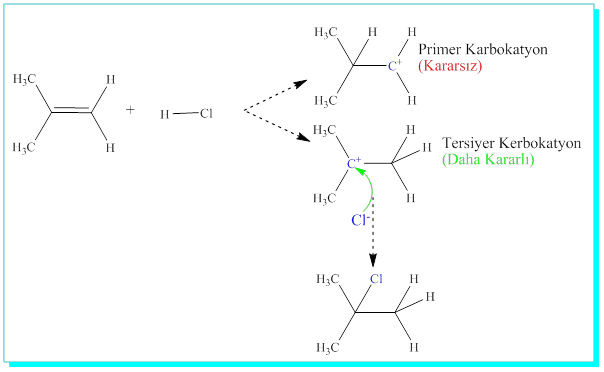
Reaksiyon mekanizmasından da görüleceği üzere, hidrojenin katılması iki tür karbokatyon oluşturur. Primer ve tersiyer, tersiyer karbokatyon daha kararlı olduğundan klor tersiyer yapıya bağlanmıştır.
S / Aşağıdaki karbokatyonları, primer sekonder, tersiyer durumlarına göre isimlendirerek kararlılık sırasına göre yazınız.
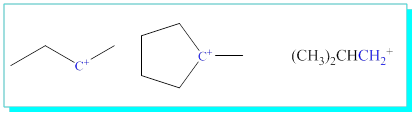
(b>a>c)
4.8-Alkenlere katılmada ANTİ-MARKOFNİKOF KURALI (BH3)
Markofnikof kuralında hidrojenin genelde bileşikler içerisinde pozitif yüklü olmasından dolayı hidrojenin çok olduğu tarafa bağlandığı unutulmamalıdır. Kararlı karbokatyon oluşturma mantığı akılda bulundurulabilir.
“Eğer hidrojenin kısmen negatif yüklü olduğu bileşikler kullanılırsa durum bunun tersidir ve hidrürler hidrojenin az olduğu tarafa katılırlar.” Anti-Markofnikof kuralı.
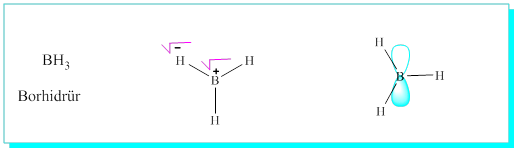
Burada bor hidrürdeki bor bir Levis asididir ve boş bir orbitali olduğundan ( açık olarak inceleyiniz) kısmen pozitif yüklüdür. Bu nedenle kısmen pozitif bor katılmada hidrojenin çok olduğu yere katılacaktır.
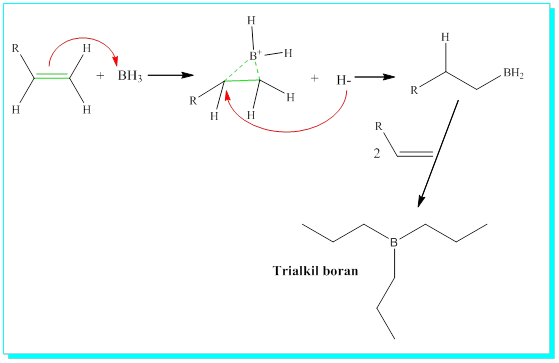
Hidroborasyon da bor üzerinde üç tane hidrojen olduğu için üç tane alken katılması olur.
Genelde oluşan ürün izole edilemez ve reaksiyonu oksidasyon takip eder.

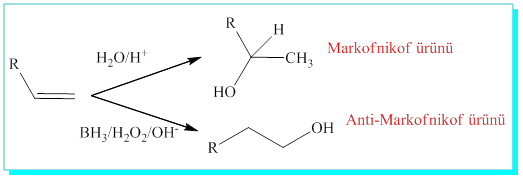
Yükseltgeme hidrojen peroksit ve sodyum hidroksit ile tamamlandığında Antimarkofnikof (hidrojenin az olduğu yere hidrür katılması) ürünü alkoller oluşur.
Böylece alkenlerden alkol elde edilişinde regioselektif (yer seçimli) olarak, normal asidik ortamda su katılması Markofnikof ürünü ya da bor hidrür ile anti Markofnikof ürününü elde edebileceğimizi anlarız.
S / Aşağıdaki reaksiyon denklemini tamamlayınız.
S / 2-Metilpropenin hidroborasyon oksidasyon ürünü nedir?

4.8-Alkenlerde Hidrojenleme Reaksiyonları
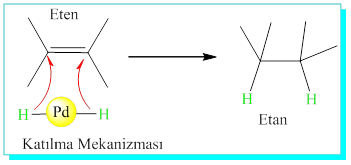
Pt ( Platin), Pd (Palladyum), Ni ( Nikel) gibi metallerin katalizi yardımı ile alkenlere hidrojen gazı katılır ve alkanları verir.

Hidrojen gazı katalizör üzerinde aktiflenir ve alkene aynı yönden katılır.

4.9-Alkenlerin permanganatla yükseltgenme reaksiyonları:
Alkenlar bazik potasyum permanganatla (KMnO4) glikolleri (1-2-diol) oluştururlar.
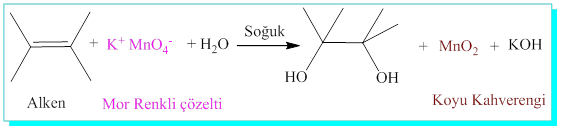
Alkenlere permanganat katılması esnasında, permanganatın mor rengi kaybolurkan siyahımsı mangan dioksit oluşurki bu rengin mordan siyaha dönme alkenlerin tanınma reaksiyonu olarak da kullanılır.
4.10-Alkanların ozonlama ( O3) reaksiyonları.
Alkenler ozon ( O3) le çok hızlı bir şekilde reaksiyon vererek ozonidleri oluştururlar ki bunlar da çok reaktif olup izole edilemezler, izolasyonları bazen patlamalara sebep olur. Ozonidler çinko ve sulu asitlerle iki karbonil ürününe parçalanır.
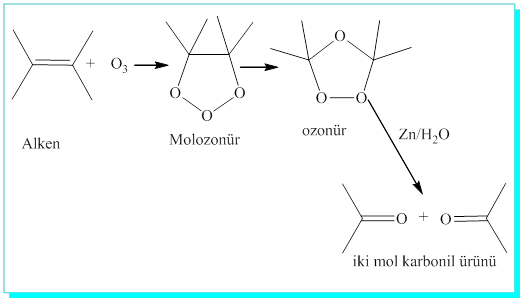
Ozonlama denen bu toplam reaksiyonda asıl sonuç, alkenin çift bağının her iki tarafına da oksijen bağlanmasıdır.
Ozonlama sonucu simetrik moleküller iki mol aynı ürünü oluştururken, simetrik olmayan alkenler de iki farklı karbonil ürünün karışımını veriler.
Örnek olarak, 2-buten iki mol etanal verirken, 1-buten bir mol formaldehit ve bir mol propanal verir.
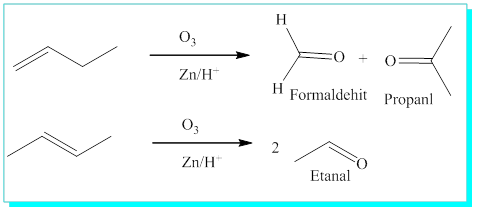
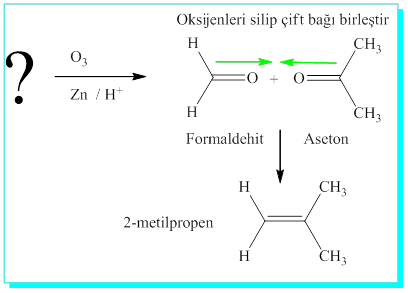
S/ Bir alkanın ozonlanması aseton (Dimetil keton) ve Formaldehit vermektedir. Parçalanma öncesi alkenin yapısı nedir.
Aseton- CH3-CO-CH3 ve Formaldehit, H2CO
5-ALKİNLER (ASETİLENLER)

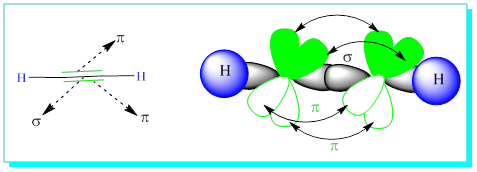
Alkinler, Asetilenler bazen kendi serilerinin ilki olan asetilene atfen asetilenler diye de bilinir. Aralarında üçlü bağ bulunan iki karbon atomunun bağlanmaya müsait sadece iki ucu kalmıştır ve bağ açısı 180° dir. Yani yukarıda gösterildiği gibi düzlemseldir ve cis-trans izomerleri yoktur. SP-hiprit orbitali yapan (ilk bölümde açıklanan hibritleşmeye tekrar bakınız) iki karbonun bir bağı hipritleşmiş SP-lerinin üst üste, diğerleri ise hipritleşmemiş P orbitallerinin karşılıklı çakışması ile oluşmuştur.
Alkenlerde gösterilen birçok katılma reaksiyonu biraz yavaş reaksiyon vermekle birlikte alkinler için de geçerlidir. Örnek olarak brom alkinlere katılarak,
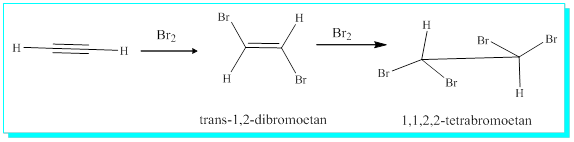
Görüldüğü gibi, ilk katılma alkenlere benzer olarak trans ürün verirken oluşan alken yine çift bağ içerdiği için tekrar katılma vererek 1,1,2,2-tetrabromoetan verir.
Alkinlerin hidrojenlenmesi de tamamen alkanlara kadar ilerlemektedir.
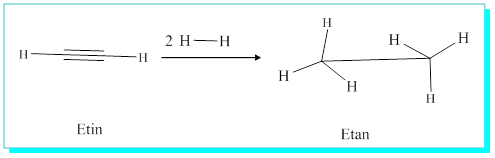
Bu durumdan kurtulmak, yani sadece bir mol hidrojen katarak “alken” durumunda kalmak da mümkündür. Tek bir pi- bağının kırılması ve birinin kalması için kullanılması gerekli olan özel bir katalizör vardır ve buda Lindlar katalizörü olarak adlandırılır.

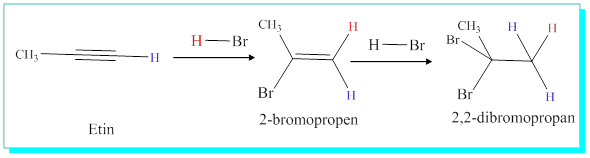
Simetrik olmayan alkinlere katılmalarda da alkenlere katılmada ki Markofnikof kuralı alkenlerde ki gibi aynen geçerlidir ve iki defa ayrı ayrı uygulanması gereklidir.
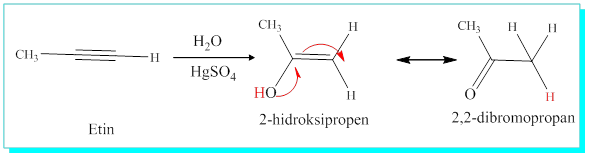
Alkinlere su katılmasında ise sadece asit yeterli olmayıp cıva iyonunun da yardımı gerekmektedir. Cıva iyonu molekülün üçlü bağıyla kompleksleşip bağı aktifler ve katılmayı kolaylaştırır. Katılma ürünü yine bir vinil alkolüdür ki buda rezonans ile daha kararlı karbonil bileşiği halini alır.
S / Aşağıdaki reaksiyon denklemlerini tamamlayınız.

Asetilenik hidrojenler (üçlü bağa direk bağlıolanlar) asidiktir ve sodyum amit (sodamit) gibi güçlü bazlar ile koparılabilirler, asetilenik yapı ise metal-ylidi denen tuzları oluşturur.
